重点监控品种阔别医保
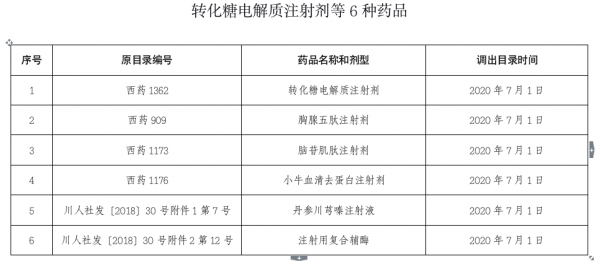
6月23日,四川省医保局发布通知称,将纳入国家重点监控范围的转化糖电解质注射剂等6种药品于2020年7月1日起调出《药品目录》。
昨日,浙江省发布《关于执行国家医保药品目录相关管理要求的通知》明确,凡列入“第一批国家重点监控合理用药药品目录”的原省医保药品目录内药品,于6月30日调整出浙江省医保支付范围。
根据通知,丹参川芎嗪、转化糖电解质、骨肽氯化钠、长春西汀葡萄糖4个国家重点监控药品被调出浙江省医保支付范围。
6月17日,国家医保局联合财政部、国家税务总局发布《关于做好2020年城乡居民基本医疗保障工作的通知》要求,今年6月底前将国家重点监控品种剔除出目录并完成40%省级增补品种的消化。
回顾一下重点监控品种从进入目录到被调出医保的历程可以发现,其实前后不过一年的时间。
2019年7月1日,《第一批国家重点监控合理用药药品目录(化药及生物制品)》正式发布,20个通用名被纳入。
紧随其后,2019年8月20日,国家医保局发布《国家医保局人力资源社会保障部关于印发国家基本医疗保险、工伤保险和生育保险药品目录的通知》明确:
各地应严格执行《药品目录》,不得自行制定目录或用变通的方法增加目录内药品,也不得自行调整目录内药品的限定支付范围。对于原省级药品目录内按规定调增的乙类药品,应在3年内逐步消化。消化过程中,各省应优先将纳入国家重点监控范围的药品调整出支付范围。
最终,根据国家医保局的要求,国家重点监控品种被调出医保的大限被定为2020年6月30日。
就此,北京鼎臣医药管理咨询中心创始人史立臣对赛柏蓝表示,针对被纳入国家重点监控的药品,不少医院本身就大幅减少了对其的使用,这些品种最终一定会退出医院,但是一个品种的退出也需要时间,所以相关部门才给了一年的过渡时间,实际上将这些品种调出医保是很容易的,但是考虑到有些省份已经签订了部分药品的采购协议,也不能直接作废,所以还是会结合实际的情况给企业和医院一些过渡期。
医院市场大受影响
米内网数据显示,在37个超10亿的地方医保产品中,有14个被纳入了国家重点监控目录——包括胸腺五肽、核糖核酸Ⅱ、转化糖电解质、神经节苷脂、小牛血清去蛋白、奥拉西坦、胸苷肌肽、曲克芦丁脑蛋白水解物、磷酸肌酸钠、复合辅酶、丹参川芎嗪,涉及企业近百家。
其中,奥拉西坦注射液、脑苷肌肽注射液、曲克芦丁脑蛋白水解物注射液、软化糖电解质注射液、注射用复合辅酶、注射用核糖核酸II、注射用奥拉西坦等是超过20个省份的地方医保增补品种。
其实在被彻底调出医保之前,由于重点监控制度,这些品种的销量已经大受影响——据米内网数据,2019年在中国公立医疗机构终端,14个国家重点监控品种的销售额增长率均为负值,其中单唾液酸四己糖神经节苷脂钠注射液、注射用复合辅酶、注射用磷酸肌酸钠下滑幅度超过30%。
在彻底阔别医保目录之后,这些重点监控品种可能还将进一步承压。
史立臣今日对赛柏蓝表示,从地方医保目录中被调出对于重点监控品种的影响是非常大的,因为被调出医保就意味着转为自费药品,而这些重点监控品种在有医保支付的时候还有一些医生和患者有意愿使用,一旦失去医保报销,患者使用的意愿会大大降低。
另外值得注意的是,因为发现自费药物可能涉及到商业贿赂等问题,各地针对自费药品的使用管理也在强化——比如上海就曾发布过相关通知要求进一步加强医药购销领域行风建设,杜绝商业贿赂违法违规行为,切实降低上海市自费药品“虚高”价格,减少不必要的自费药品采购和使用。
他进一步指出,更有甚者有些省市甚至会出台规定要求,医生给患者开具自费药品,需要患者签字同意。
国家重点监控药品目录调整
在发布第一批重点监控药品目录时,国家卫健委曾明确表示,将定期对全国辅助用药目录进行调整,调整时间间隔原则上不短于1年。
到今年7月,距离第一批重点监控药品目录公布的时间间隔刚好一年,下一批重点监控药品目录会否公布、何时公布自然也成为了业内需要关注的问题。
就此,史立臣对赛柏蓝说,仔细看一下全国各省市的重点监控药品目录不难发现,有不少省市的重点监控品种都不止20个,即便合并去重,最后剩下来的总数也依然相当庞大,加之国家第一批重点监控药品目录仅纳入了20个品种,后续相关部门继续公布下一批的重点监控药品目录也是大概率事件。
那哪些品种被纳入目录的可能性比较大呢?在史立臣来看,药品的临床价值,是否进入医院诊疗路径,药品的安全性、有效性,药物经济学的相关角度等是相关部门确定重点监控药品目录时考虑的主要方面。
除上述因素外,药品的使用量、使用金额可能也是纳入考虑的指标之一。
2018年12月12日,国家卫健委发布《关于做好辅助用药临床应用管理有关工作的通知》指出,将制订全国辅助用药目录。
彼时国家卫健委给出的要求是二级以上医疗机构将本机构辅助用药以通用名并按照年度使用金额由多到少排序,形成辅助用药目录。
先重点监控,再调出医保
在印发《第一批国家重点监控合理用药药品目录(化药及生物制品)的通知》之初,针对重点监控品种,国家卫健委要求,对纳入目录中的全部药品开展处方审核和处方点评,加强处方点评结果的公示、反馈及利用。对用药不合理问题突出的品种,采取排名通报、限期整改、清除出本机构药品供应目录等措施,保证合理用药。
不久,国家医保局就发布文件明确将国家重点监控品种调出医保,上述管理办法也成了过渡性举措。
随着国家重点监控目录和医保目录的动态调整,似乎重点监控药品目录和医保目录调整之间会形成联动,被纳入重点监控目录的药品大概率也难逃脱被调出医保的命运。
就两者之间的联动关系,国家医保局医药服务管理司司长熊先军也表示:“从调出的品种来看,有一些是年销售量比较大的品种,将此类药品调出目录,有利于为调入更多救命救急的好药腾出空间,也有利于促进行业加快转型升级。”
史立臣认为可能只需要两年左右的时间,部分药品的调整工作就能完成。也就是说,虽然重点监控药品目录短期内涉及的品种仍然较少,但是持续下去的话,影响的品种会越来越多,对于企业的影响也会非常大。
他表示,一些药企不做研发,只有投机心理,认为政策有松有紧,这类企业难以有长期的发展前景。史立臣建议药企如果从立足产品的角度出发,可以做临床,明确产品的临床价值;或者联合用药发挥好产品的功效;亦或开发产品新的适应症。从企业战略的角度出发,如果相关品种进入了重点监控目录,企业就需要明确还有哪些省份的市场可以做,作为现金流品种,尽量稳住销售,然后逐渐用其他品种代替这些产品。
